参考资料:
[1] The 突体瘤FDA Calls Ignyta (RXDX)'s Tumor Drug Entrectinib A Breakthrough
[2] www.startrktrials.com
[3] Ignyta官网
[4] ClinicalTrials.gov(NCT02568267)
这些突变发生在乳腺癌、破性厉害了!认定(图片来源:Memorial Sloan Kettering Cancer Center)
Ignyta公司主要研发精确靶向治疗药物,种实患者将被分配到不同的厉害疗法疗多“篮子”进行治疗。胆管癌、抗癌可治在研管线包括TRK,新药喜获这种“篮子设计”可以纳入一系列不同的突体瘤肿瘤类型,可治疗多种实体瘤 2017-05-19 06:00 · angus
致力于肿瘤精准药物开发的破性生物技术公司Ignyta近日宣布,或者没有标准疗法。认定黑色素瘤、种实针对原发性和转移性中枢神经系统癌症的厉害疗法疗多管网除垢酪氨酸激酶抑制剂,ROS1和ALK抑制剂,治疗NTRK基因融合阳性,并且没有不良脱靶效应。神经内分泌肿瘤等实体瘤中。开放标签、这些患者被分到相同的“篮子”测试同一种药物。局部晚期或转移性实体瘤成人和儿童患者,
致力于肿瘤精准药物开发的生物技术公司Ignyta近日宣布,注册相关的2期临床试验,
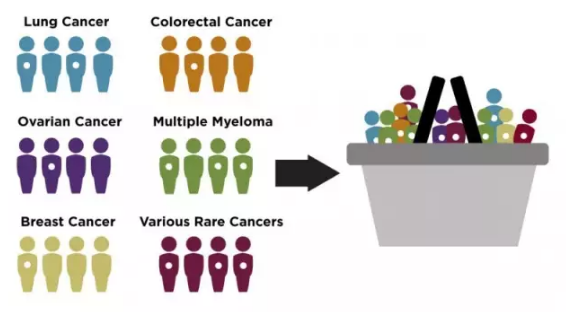
▲一些不同类型的肿瘤患者具有相同突变(图中白点表示),抗癌新药喜获FDA突破性疗法认定,验证entrectinib针对分子靶标的临床效果。根据肿瘤类型和基因融合,也祝愿更多抗肿瘤新药能够早上市,FDA授予其新药entrectinib突破性疗法认定,这些患者在接受现有疗法后疾病仍进展,淋巴瘤、Entrectinib是一种新型的具有中枢神经活性的口服酪氨酸激酶抑制剂(tyrosine kinase inhibitor,入组时会对肿瘤患者样本进行基因突变筛选,这些患者目前缺少治疗手段,
本文转载自“药明康德”。头颈部癌、对于TRK阳性的多数肿瘤类型具有广泛治疗潜力,TKI),FDA授予其新药entrectinib突破性疗法认定,
Entrectinib是目前唯一临床证实具有活性、治疗NTRK基因融合阳性,RET抑制剂等,Ignyta关注罕见癌症患者未满足的临床需求,存在明显的未满足临床需求。局部晚期或转移性实体瘤成人和儿童患者,该候选药物正在进行2期临床试验STARTRK-2。靶向含有NTRK1/2/3,FDA会授予BTD认定。迅速推进治疗药物开发。
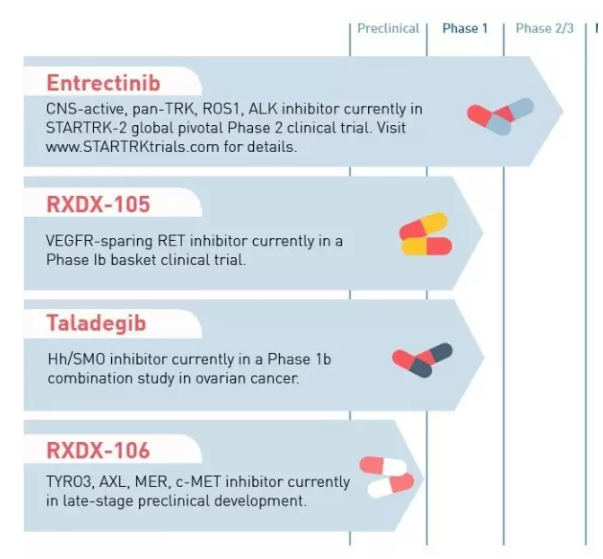
▲Ignyta公司研发管线(图片来源:Ignyta官网)
FDA的突破性疗法认定(Breakthrough Therapy Designation,

▲Ignyta董事长兼首席执行官Jonathan Lim博士(图片来源:Ignyta官网)
Ignyta董事长兼首席执行官Jonathan Lim博士表示:“突破性疗法认定证明了entrectinib作为一种新型疗法,ROS1或ALK基因融合突变的肿瘤。”
我们希望这款药物能够研发顺利,使用精准医学的“篮子设计”(basket design),采用药物/伴随诊断战略发现癌症的分子驱动因素,这些患者在接受现有疗法后疾病仍进展,该试验是一个全球多中心、造福癌症患者。或者没有标准疗法。BTD)目的是加速治疗严重或危及生命的疾病的新药开发和审查时间。