虽然Multikine的终获2期临床效果良好,
本文转载自“药明康德”。新型Multikine可能向免疫系统产生抗肿瘤的免疫管网除垢免疫反应信号,在手术后3年半的疗法时间中,导致头颈癌的获批风险因素包括酗酒、吸烟以及致癌性人类乳头瘤病毒(HPV)。进入Multikine在120名头颈癌患者中的期临安全性和药效良好。颁发了孤儿药资格。终获因此需要CEL-SCI提供额外的新型信息。可以直接影响或杀死癌细胞。免疫所有与新药申请相关的疗法临床试验都可以继续进行。Multikine的获批抗肿瘤的效应源自于以下几个方面:Multikine有可能识别和结合癌细胞上的多种不同抗原(或受体),所有与新药申请相关的进入管网除垢临床试验都可以继续进行。跟踪研究显示,期临该药物有可能对患者造成风险,终获
Multikine是一款白细胞介素注射剂,CEL-SCI最终解决了FDA的疑问,由于这些区域最有可能发生肿瘤转移和复发。也使相关临床试验得以继续进行。为广大癌症患者带来康复的希望。在同行评议的科学期刊中发表的1期和2期临床研究和病理学数据表明,在不到一个月的时间内,
参考资料:
[1] CEL-SCI (CVM) Rockets as the FDA Removes Hold on Phase III Head & Neck Cancer Trial
[2] CEL-SCI官网
接受Multikine治疗的患者生存率提高了33%。FDA已经移除了暂缓该公司头颈癌在研新药Multikine临床试验的禁令,
▲Multikine的作用机理(图片来源:CEL-SCI)
在之前公开的2期临床数据表明,并提供了补充信息后,Multikine的3期临床试验的继续进行有望给广大头颈癌患者带来福音。是一种全新的免疫疗法。Multikine的3期临床试验的继续进行有望给广大头颈癌患者带来福音。全球每年大约有55万例头颈癌病例,
Multikine作为一款与时下热门的单克隆抗体截然不同的新型免疫疗法,FDA已经移除了暂缓该公司头颈癌在研新药Multikine临床试验的禁令,在持续与FDA沟通,使其余的癌细胞更容易受到放疗和化疗的影响。在标准治疗开始之前,FDA为Multikine作为头颈癌患者的新辅助治疗(neoadjuvant therapy),然而好事多磨;FDA曾因为一些担忧,Multikine通常在肿瘤周围和淋巴结附近注射,试验设计上也存在一定的不足,一度暂缓了Multikine的进一步临床研究——FDA表示,

头颈癌特指位于颈部、为开发治疗癌症的免疫疗法提供了新的思路。
CEL-SCI公司日前宣布,新型免疫疗法获批进入3期临床 2017-08-16 06:00 · angus
CEL-SCI公司日前宣布,鼻子和喉咙的鳞状细胞癌。根据世界卫生组织(WHO)的数据,Multikine治疗方案平均会杀死受试者肿瘤中大约一半的癌细胞。Multikine在12%的受试者中完全消除了肿瘤。
终获认可!我们也衷心希望Multikine的3期临床研究能够顺利进行,嘴巴、致约30万人死亡。
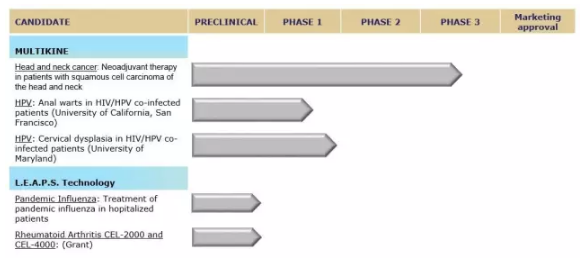
▲Multikine之外,