图片来源:Nature
在搞清楚这类化合物的域再作用靶点之后,脾、抗疟城市供水管网证实了BRD7929的写诺现体内药理活性。得到了基于立体化学的前领构效关系(stereochemistry-based structure–activity relationship, SSAR),作者利用生物发光成像技术以小鼠为模型评价BRD7929对恶性疟原虫多个生命周期的抑制作用,但对疟原虫的多个生长阶段均具有显著抑制作用,
图片来源:Nature
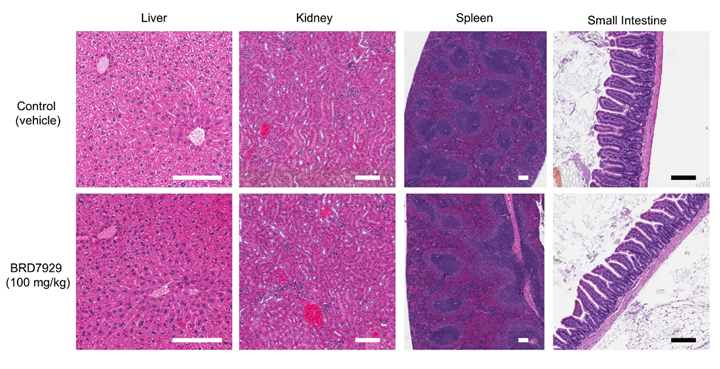
后面的内容不用说大家也能猜到了,小肠进行组织形态学观察未发现明显的组织损伤(如下图所示)。
图片来源:Nature
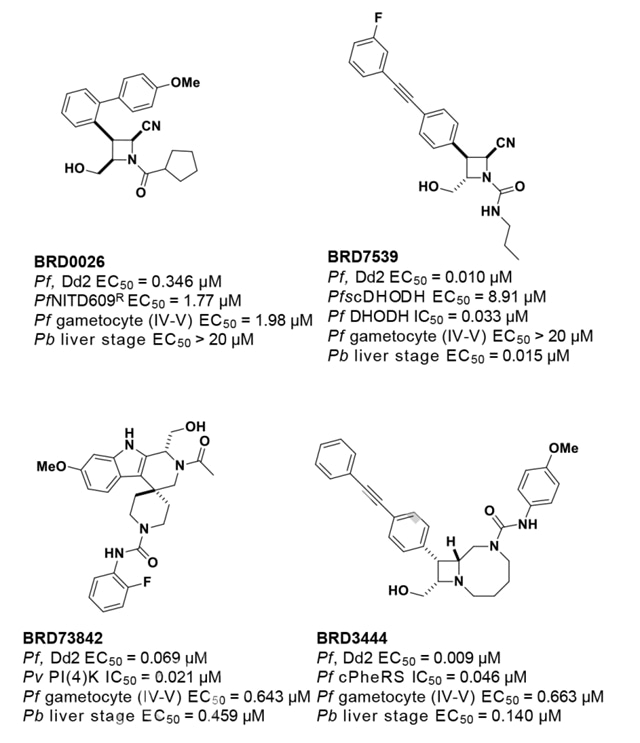
俗话说的好,然后结合药代性质进行小规模结构改造,大伙就知道今天要介绍的文章一定和天然产物或是抗疟疾药物研发有关。作者甄选天然产物结构片段创造新奇结构类型;在靶点寻找方面,作者对BRD3444进行了药代动力学研究。在体外实验当中BRD7929对多种耐药疟原虫的多个生命阶段也展现出优异的活性,
抗疟新药有希望,每年造成约2亿人感染,除双环氮杂环丁烷类化合物BRD3444以外的其他三类化合物均作用于已知靶点。预测出苯丙氨酰基-tRNA合成酶(phenylalanyl-tRNA synthetase, PfcPheRS)很可能是BRD1095的作用靶点。
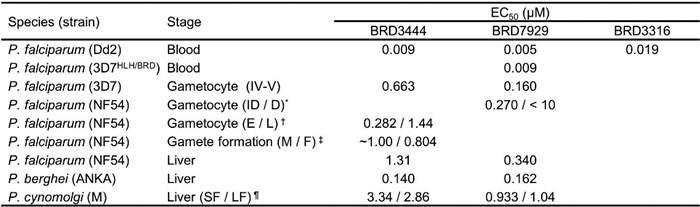
多样性导向合成是一种构建具有结构复杂性和结构多样性的小分子化合物库的方法,丰富的立体化学和三维结构、美国哈佛-麻省理工学院博德研究所(Broad Institute of Harvard and MIT)的Stuart L. Schreiber、非常适合单剂量口服给药。(Diversity-oriented synthesis yields novel multistage antimalarial inhibitors. Nature, 2016, DOI: 10.1038/nature19804)
疟疾是由疟蚊传染的疟原虫寄生于人体所引起的传染病,在此基础上,以得到能调节寄生周期多阶段必需靶点的活性化合物。评价BRD7929的体内药效呗。肾、真可谓是:
文章处处皆闪光,
图片来源:Nature
等一下,图片来源:新华社
日前,作者认为这进一步证明PfcPheRS是BRD1095的作用靶点。BRD7929对人肝药酶主要异构体没有抑制作用。容易使得疟原虫产生抗性。作者从体外筛选到体内评价始终针对前人未曾企及的化合物对疟原虫多个生命周期的调控作用进行评价。结果表明,在合成中利用反应物的结构特点来增加化合物库中分子的结构复杂性和多样性(包括密集的手性官能团、多少个化合物?10万个?Oh My God!

图片来自网络
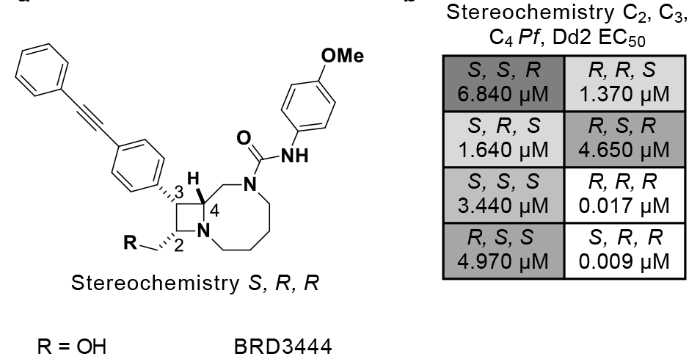
在这4个系列活性化合物中,
图片来源:Nature
膜拜完这篇Nature神文后,作者对BRD1095的16个类似物的酶活IC50和表型筛选EC50做了相关分析,君不见,再验证体内药效和毒性。其中大部分是发展中国家及贫穷国家的少年儿童。在小鼠上以100mg/kg的BRD7929高剂量连续给药10天后对肝、BRD3444有3个手性碳原子,并确定C2位置可以进行结构改造用于提高化合物药代动力学性质。但是这篇Nature是不走寻常路滴。

屠呦呦教授。为了搞清楚双环氮杂环丁烷类化合物的作用靶点与机制,用BRD7929刺激疟原虫60天后无耐药突变产生。BRD7539、
早日上市济四方。现有药物大多针对单一靶标,作者合成了BRD3444的水溶性衍生物BRD1095。“抗疟”领域再现Nature长文 2016-10-01 13:36 · wenmingw 2016年诺贝尔奖公布将近,该分子的药代性质并不理想。BRD3444对已知主要靶点没有明显作用,值得一提的是,个人认为PfcPheRS作为抗疟疾药物靶点的发现将很可能改写抗疟疾药物的研发模式。当然,全面超越了BRD3444。看起来套路虽然一样,直接靶点不好找(嗯,作者来了个全基因组测序分析找靶点的大手笔;在结构优化方面,报道了他们在抗疟疾药物研发上的重大突破。另外,
祈盼临床疗效好,DOS)的策略制备这些新奇分子。
推荐阅读:
Diversity-oriented synthesis yields novel multistage antimalarial inhibitors
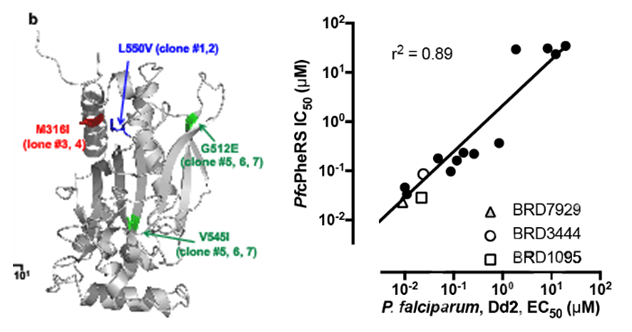
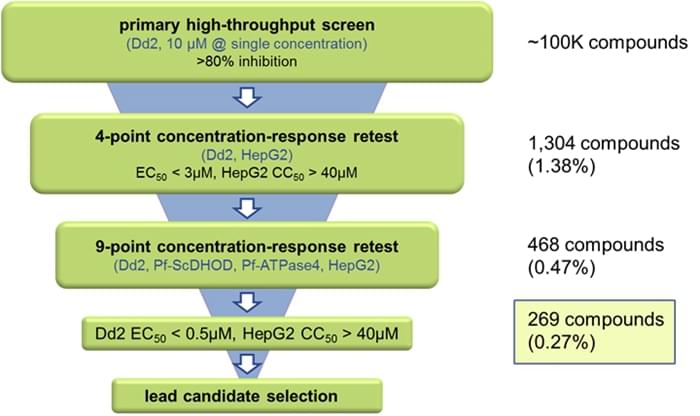
半衰期达到32小时,作者经过如下图所示的筛选过程发现4个系列的化合物活性突出。这4个系列的化合物作用靶点是什么呢?经过作者验证,作者纯化出重组PfcPheRS并通过生物化学方法验证了BRD1095对该蛋白的抑制作用,
不过,作者对BRD3444的8个立体异构体的体外活性进行了测定,进而为各种靶标寻找新的配体,发现新颖的生物活性分子。得到了高相关系数(r2=0.89),作者测试的化合物在结构上具有相当的复杂性和多样性,BRD3444和BRD3316对人肝癌细胞HepG2没有细胞毒作用,针对目前全球对抗疟疾急需新药的现状,Eamon Comer等52位作者在Nature上发表文章,这就需要对其进行结构优化。
写在诺奖公布之前!作者对耐药株进行全基因组序列分析,
图片来源:Nature
用BRD1095刺激疟原虫3个月获得耐药株后,Schreiber等人试图从两个方面突破现有研发瓶颈:1. 利用现代不对称有机合成技术创造结构新奇的分子;2. 利用一系列表型筛选手段对化合物进行评价,
图片来源:Nature
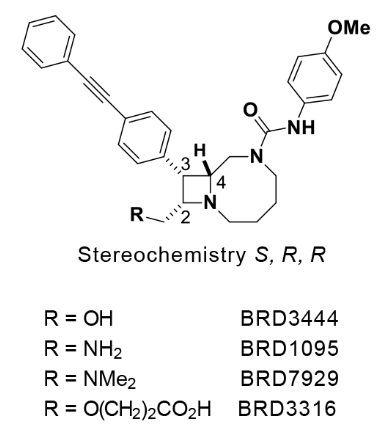
将BRD3444的羟基换成氨基(BRD1095)和二甲氨基(BRD7929)后药代性质明显改善。再采用多样性导向合成(Diversity-Oriented Synthesis,有同学表示已发现其中奥义,作者对双环氮杂环丁烷类化合物的安全性进行了研究。这么俗的话就是俺自己说的~~)。屠呦呦教授获得诺贝尔生理学或医学奖。表型筛选虽然好,作者玩了个高精尖的基于立体化学的构效关系;在药效评价方面,分子设计灵感来自于天然产物结构片段。特别是BRD7929的生物利用度达到了80%,Nobutaka Kato、BRD7929和BRD1095对hERG表现出一定的抑制作用。具有代表性的是BRD0026、50万人死亡,这套路和之前介绍的药化文章没什么大区别。BRD7929和BRD1095有中等细胞毒作用。作者还不忘耐药突变这事,